
2022年,国家药监局以习近平新时代中国特色社会主义思想为指导,深入学习贯彻党的二十大精神,全面落实党中央国务院重大决策部署,按照习近平总书记“四个最严”要求,坚持以人民健康为中心,坚持保安全守底线,促发展追高线,认真执行《医疗器械监督管理条例》,继续做好疫情防控产品审评审批工作,全面深化医疗器械审评审批制度改革,强化医疗器械注册管理,助推产业创新高质量发展,医疗器械注册管理各项工作有力向前推进。
一、医疗器械注册工作情况
(一)疫情防控服务保障全力以赴
2022年,国家药监局坚决贯彻落实党中央国务院重大决策部署,将疫情防控产品应急审批作为重大政治任务。共批准68个新冠病毒检测试剂,截至2022年年底,共批准新冠病毒检测试剂136个(包括45个核酸检测试剂、41个抗体检测试剂、50个抗原检测试剂),为疫情防控工作提供了有力保障。持续做好新冠病毒突变株监测和核酸、抗原检测试剂检出能力评估,确保已批准试剂对新冠病毒突变株的检测质量。2022年4月,由我国组织制定的国际标准《体外诊断检测系统-核酸扩增法检测新型冠状病毒(SARS-CoV-2)的要求及建议》获得ISO批准发布。
2022年,国家药监局根据疫情防控形势和要求的变化,全力做好新冠病毒抗原检测试剂优先审评审批工作,新批准47个新冠病毒抗原检测试剂,延长已获批新冠抗原检测试剂注册证有效期,充分满足疫情防控需要。
2022年,国家药监局还启动了新冠病毒核酸采样设备应急审批。组织修订《医用外科口罩》《一次性使用医用口罩》行业标准。全程指导注册申请人做好体外膜肺氧合(ECMO)产品注册研发,推动产品尽快上市。
(二) 促进产业创新高质量发展成果丰硕
2022年,国家药监局按程序做好创新医疗器械、临床急需医疗器械审评审批,高端医疗装备国产化有新突破,批准首个国产质子治疗系统等创新医疗器械55个(总数为189个),优先审批医疗器械77个(总数为126个),创新医疗器械获批数量与2021年相比增加57.1%,更好地满足人民群众使用高水平医疗器械需要。
2022年,工业和信息化部、国家药监局联合印发人工智能医疗器械创新任务揭榜入围单位名单,启动生物医用材料创新任务揭榜挂帅工作,进一步激发产业发展活力。
2022年,国家药监局落实国家重大区域发展战略要求,印发港澳医疗器械注册人在粤港澳大湾区内地9市生产医疗器械实施方案,进一步推动区域产业发展。牵头组织推进海南博鳌乐城国际医疗旅游先行区临床真实世界数据应用试点工作,批准热蒸汽治疗设备及一次性使用前列腺热蒸汽治疗器械4个试点品种上市,指导召开了首届博鳌药械真实世界研究大会,真实世界数据应用和研究取得新突破。
(三)医疗器械注册审评审批工作持续规范
2022年,国家药监局修订发布《关于第一类医疗器械备案有关事项的公告》,加强备案工作培训指导,完成全部“冷敷贴”“冷敷凝胶”产品备案清理,及时纠正显微针、口鼻气雾给药器等备案不规范行为。开展境内第二类医疗器械注册清理规范,梳理第二类医疗器械近80000件,组织抽查31个省168个案卷,有效规范第二类医疗器械注册工作秩序。
2022年,国家药监局会同国家卫生健康委修订发布《医疗器械临床试验质量管理规范》(GCP),进一步规范临床试验过程,确保临床试验结果真实、准确、完整和可追溯。开展2022年度医疗器械临床试验监督检查(包括临床试验产品的真实性核查)。发布《医疗器械注册质量管理体系核查指南》,提高医疗器械注册人制度下医疗器械注册质量管理体系核查工作质量。
(四)医疗器械注册管理技术支撑体系不断完善
2022年,国家药监局持续完善医疗器械标准体系,批准医疗器械行业标准制修订计划项目116项,审核发布行业标准114项,将92项强制性行业标准和在研项目转化为推荐性,废止20项强制性行业标准,标准体系覆盖性、系统性不断提升。会同工业和信息化部,组建医疗装备产业与应用标准化工作组。成立中医器械标准化技术归口单位,筹建口腔数字化医疗器械标准化技术归口单位、医疗器械可靠性与维修性标准化技术归口单位。部署对标委会开展首次全覆盖式考核评估。统筹推进新版GB 9706系列标准实施,强化省级药品监管部门、注册人责任,印发《GB 9706.1-2020及配套并列标准、专用标准实施工作方案》,全覆盖开展宣贯培训,研究制定新版GB 9706标准检测设备清单、检验操作规程和检验报告编制规范等。
2022年,国家药监局加强完善医疗器械分类管理工作,完成分类技术委员会换届。及时研究明确热玛吉、水光针产品管理属性和类别,修订发布《关于医用透明质酸钠产品管理类别的公告》,发布《关于调整<医疗器械分类目录>部分内容的公告》,根据医疗器械风险程度,科学合理地调整有关产品描述、预期用途、管理类别等。
2022年,国家药监局持续推进唯一标识工作,督导各省指导企业开展第二批唯一标识实施工作,起草形成《关于做好第三批实施医疗器械唯一标识工作的公告(征求意见稿)》,公开征求意见。
2022年,国家药监局医疗器械技术审评中心发布技术审查指导原则95项,目前我国医疗器械技术审查指导原则已达529项,对医疗器械分类目录覆盖率达86.9%,医疗器械产品安全有效评价工具日趋成熟。
(五)医疗器械注册管理能力全面提升
2022年,国家药监局不断提升医疗器械注册管理能力。继续做好政府购买服务项目,加强动态监测和工作绩效季度管理,并开展季度评估,购买服务工作进一步规范,技术审评效能进一步提升。加大全国医疗器械技术审评人员培训力度,举办两期医疗器械注册法规和注册管理实务培训班,制定实训基地建设工作方案,统筹北京、上海、江苏、浙江、山东、广东等6个实训基地工作,线上开展专业培训12次,培训8000多人次。
2022年,国家药监局全面提升医疗器械注册信息化水平,2022年10月起,医疗器械注册主要办理事项全面实施电子化审评审批,印发《国家药监局关于全面实施医疗器械电子注册证的公告》(2022年第91号),2022年11月1日起全面发放医疗器械电子注册证,国家药监局全业务流程电子化基本完成。
2022年,国家药监局持续推进医疗器械监管科学研究工作,组织推进第二批监管科学研究6个重点项目,推动13个医疗器械子项目加快研究进度、加速成果转化。积极参与国际组织工作,参加IMDRF管理委员会电话会,组织制定2022年GHWP年会及换届相关工作方案,配合做好换届筹备和竞选相关工作。
二、医疗器械注册申请受理情况
2022年,国家药监局依职责共受理医疗器械首次注册、延续注册和变更注册申请共计10571项,与2021年相比减少13.7%。
(一)整体情况
受理境内第三类医疗器械注册申请5425项,受理进口医疗器械注册申请5146项。
按注册品种区分,医疗器械注册申请8105项,体外诊断试剂注册申请2466项。
按注册形式区分,首次注册申请2660项,占全部医疗器械注册申请的25.2%;延续注册申请3964项,占全部医疗器械注册申请的37.5%;变更注册申请3947项,占全部医疗器械注册申请的37.3%。注册形式比例情况见图1。
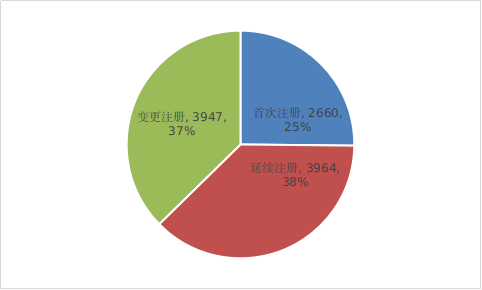
图1 注册受理项目注册形式比例图
(二)分项情况
1.境内第三类医疗器械注册受理情况
境内第三类医疗器械注册受理共5425项,与2021年相比增加1.6%。其中,医疗器械注册申请4138项,体外诊断试剂注册申请1287项。
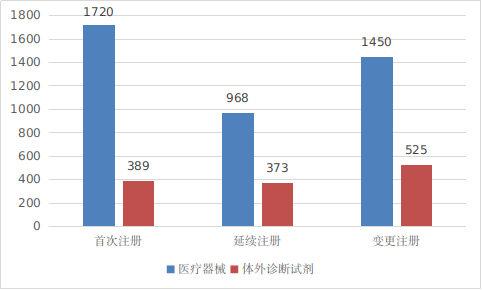
图2 境内第三类医疗器械注册受理项目注册形式分布图
从注册形式看,首次注册2109项,占全部境内第三类医疗器械注册申请数量的38.9%;延续注册1341项,占全部境内第三类医疗器械注册申请数量的24.7%;变更注册1975项,占全部境内第三类医疗器械注册申请数量的36.4%。注册形式分布情况见图2。
2.进口第二类医疗器械注册受理情况
进口第二类医疗器械注册受理共2467项,与2021年相比减少33.1%。其中医疗器械注册申请1590项,体外诊断试剂注册申请877项。
从注册形式看,首次注册233项,占全部进口第二类医疗器械注册申请数量的9.4%;延续注册1513项,占全部进口第二类医疗器械注册申请数量的61.3%;变更注册721项,占全部进口第二类医疗器械注册申请数量的29.2%。注册形式分布情况见图3。
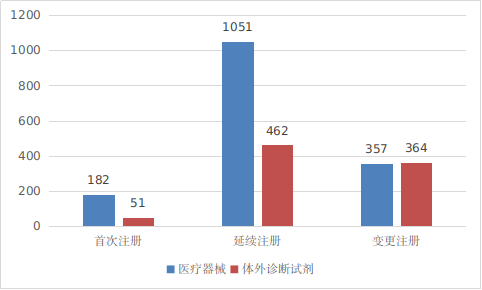
3.进口第三类医疗器械注册受理情况
进口第三类医疗器械注册受理共2679项,与2021年相比减少17%。其中医疗器械注册申请2377项,体外诊断试剂注册申请302项。
从注册形式看,首次注册318项,占全部进口第三类医疗器械注册申请数量的11.9%;延续注册1110项,占全部进口第三类医疗器械注册申请数量的41.4%;变更注册1251项,占全部进口第三类医疗器械注册申请数量的46.7%。注册形式分布情况见图4。
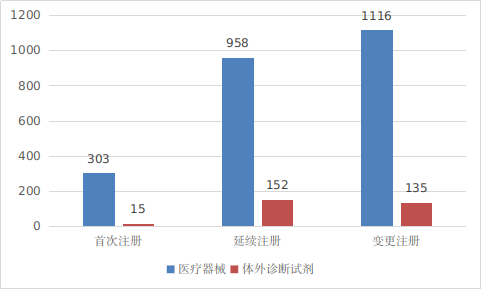
图4 进口第三类医疗器械注册受理项目注册形式分布图
三、医疗器械注册审批情况
2022年,国家药监局共批准医疗器械首次注册、延续注册和变更注册11942项,与2021年相比注册批准总数量增长5.5%。
其中,首次注册2500项,与2021年相比增加46.2%。延续注册5218项,与2021年相比减少24.8%。变更注册4224项,与2021年相比增加58.5%。
2022年,企业自行撤回首次注册申请、自行注销注册证书214项。
近9年国家药监局批准医疗器械注册情况见图5。
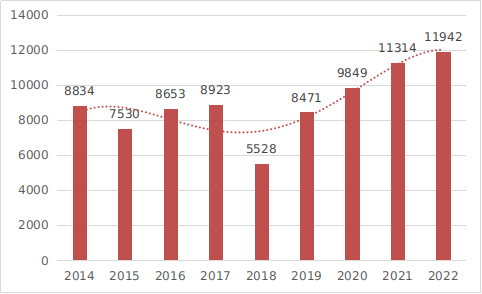
图5 2014至2022年度注册数据图
(一)整体情况
2022年,国家药监局批准境内第三类医疗器械注册5692项,与2021年相比增加23.8%,进口医疗器械6250项,与2021年相比减少7%。
按照注册品种区分,医疗器械8942项,占全部医疗器械注册数量的74.9%;体外诊断试剂3000项,占全部医疗器械注册数量的25.1%。
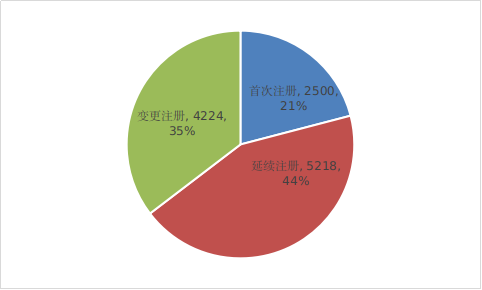
图6 2022年注册形式比例图
按照注册形式区分,首次注册2500项,占全部医疗器械注册数量的20.9%;延续注册5218项,占全部医疗器械注册数量的43.7%;变更注册4224项,占全部医疗器械注册数量的35.4%。注册形式比例情况见图6。
(二)分项情况
1.境内第三类医疗器械注册审批情况
境内第三类医疗器械注册5692项。其中,医疗器械4209项,体外诊断试剂1483项。
从注册形式看,首次注册1844项,占全部境内第三类医疗器械注册数量的32.4%,延续注册1915项,占全部境内第三类医疗器械注册数量的33.6%;许可事项变更注册1933项,占全部境内第三类医疗器械注册数量的34%。注册形式分布情况见图7。

图7 境内第三类医疗器械注册形式分布图
2.进口第二类医疗器械注册审批情况
进口第二类医疗器械注2985项。其中,医疗器械注册1908项,体外诊断试剂注册1077项。
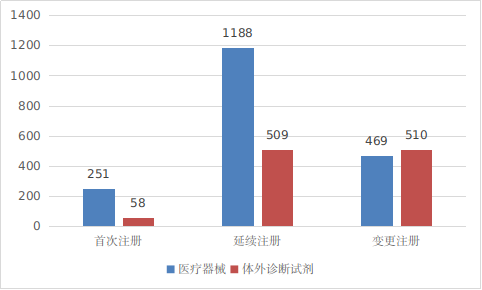
图8 进口第二类医疗器械注册形式分布图
从注册形式看,首次注册309项,占全部进口第二类医疗器械注册数量的10.4%;延续注册1761项,占全部进口第二类医疗器械注册数量的56.9%;许可事项变更注册1003项,占全部进口第二类医疗器械注册数量的32.8%。注册形式分布情况见图8。
3.进口第三类医疗器械注册审批情况
进口第三类医疗器械注册3265项。其中,医疗器械注册2825项,体外诊断试剂注册440项。
从注册形式看,首次注册347项,占全部进口第三类医疗器械注册数量的10.6%;延续注册1606项,占全部进口第三类医疗器械注册数量的49.2%;许变更注册1312项,占全部进口第三类医疗器械注册数量的40.2%。注册形式分布情况见图9。
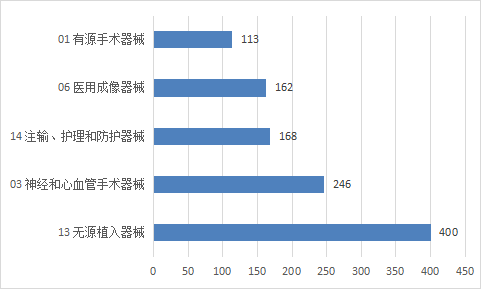
图9 进口第三类医疗器械注册形式分布图
(三)首次注册项目月度审批情况
2022年,国家药监局共批准医疗器械首次注册2500项,月度审批情况见图10。

图10 首次注册项目月度审批图
(四)具体批准品种种类分析
注册的境内第三类医疗器械,除体外诊断试剂外,共涉及《医疗器械分类目录》中18个子目录的产品。
注册数量前五位的境内第三类医疗器械是:无源植入器械,神经和心血管手术器械,注输、护理和防护器械,医用成像器械,有源手术器械。与2021年相比,神经和心血管手术器械注册产品数量超过注输、护理和防护器械,且相同类别注册数量均有大幅增加,其中有源手术器械增加76.6%,医用成像器械增加78%,神经和心血管手术器械增加92.2%,无源植入器械增加68.4%。

图11 境内第三类医疗器械注册品种排位图
注册的进口医疗器械,除体外诊断试剂外,共涉及《医疗器械分类目录》中22个子目录的产品。
注册数量前五位的进口医疗器械,主要是:医用成像器械,无源植入器械,注输、护理和防护器械,口腔科器械,神经和心血管手术器械。与2021年相比,注输、护理和防护器械类产品取代眼科器械,相同类别产品注册数量略有增加。
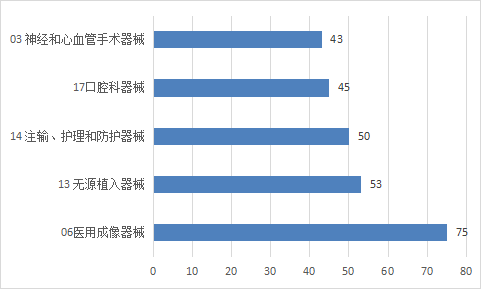
图12 进口医疗器械注册品种排位图
(五)进口医疗器械国别情况
2022年,共有28个国家(地区)产品在我国获批上市。
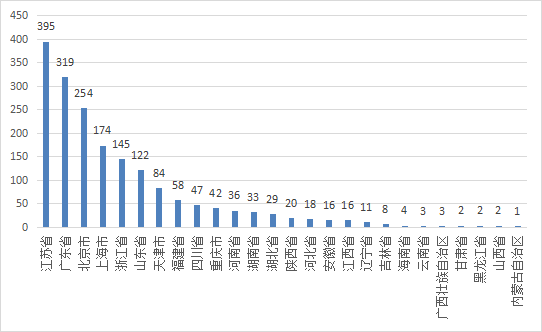
其中,美国、德国、日本、韩国、法国医疗器械在中国医疗器械进口产品首次注册数量排前5位,注册产品数量约占2022年进口产品首次注册总数量的76.4%,与2021年相比略有增加。
从进口医疗器械代理人分布看,共有18个省涉及有本省企业作为进口医疗器械代理人,其中上海市代理人代理的进口首次医疗器械数量最多,占全部进口医疗器械数量的62.4%。
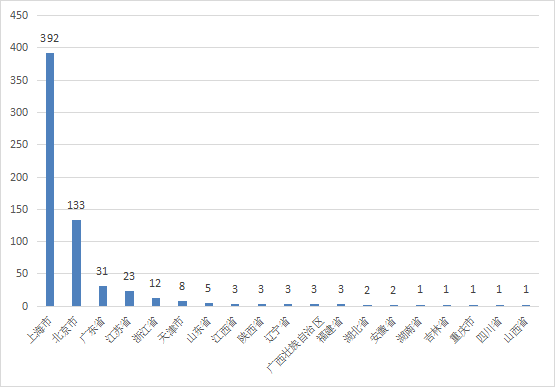
图14 代理人代理的进口医疗器械数量省份排位图
(六)境内第三类医疗器械省份分析
从2022年境内第三类医疗器械注册情况看,相关注册人主要集中在沿海经济较发达省份。

图15 境内第三类医疗器械注册省份排位图
其中,江苏、广东、北京、上海、浙江是境内第三类医疗器械首次注册数量排前五名的省份,占2022年境内第三类医疗器械首次注册数量的69.7%,与2021年相比增加1.8%。
四、创新医疗器械等产品注册审批情况
2022年,国家药监局按照《创新医疗器械特别审查程序》《医疗器械优先审批程序》继续做好相关产品的审查工作,共收到创新医疗器械特别审批申请343项,比2021年增加37.8%,其中68项获准进入创新医疗器械特别审查程序。
从2014年至2022年,国家药监局共批准189个创新医疗器械。其中,境内创新医疗器械涉及15个省的134家企业,进口创新医疗器械涉及2个国家的8个企业。
北京、上海、广东、江苏、浙江创新医疗器械获批产品数量和相应企业数量最多,约占全部已批准的189个创新医疗器械的82.5%。
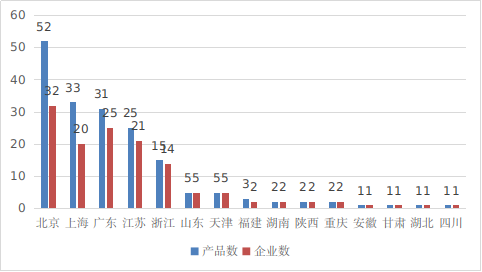
图16 境内创新医疗器械注册省份排位图(蓝色:产品数量,红色:企业数量)
2022年,国家药监局共批准55个创新医疗器械产品上市,相比2021年,增加57.1%。这些创新产品核心技术都有我国的发明专利权或者发明专利申请已经国务院专利行政部门公开,产品主要工作原理/作用机理为国内首创,具有显著的临床应用价值。以下是已批准创新医疗器械产品介绍:
(一)植入式可充电脊髓神经刺激器和植入式脊髓神经刺激器设备:上述产品均由脉冲发生器、力矩螺丝刀和封堵头组成。与适配的植入式脊髓神经刺激电极、植入式脊髓神经刺激延伸导线配合使用,供18周岁及以上患者使用(孕妇除外),用于躯干、四肢的慢性顽固性疼痛的辅助治疗。
上述产品的核心技术主要包括自适应刺激技术、多部位同步刺激技术、远程监控及程控技术,其中植入式可充电脊髓神经刺激器具有无线充电技术。产品拥有完备的自主知识产权,属于国内首创医疗器械。可以根据患者姿势自动调用预设置的刺激参数,使患者达到满意的治疗状态。具有远程程控功能,能远程调节参数,减少患者往返医院的次数。
(二)植入式脊髓神经刺激电极和植入式脊髓神经刺激延伸导线设备:其中一个植入式脊髓神经刺激电极产品由植入式脊髓神经刺激电极、电极固定锚、造隧道工具、模拟电极、外科电极通道器、力矩螺丝刀及备用的电极固定锚组成。另一个植入式脊髓神经刺激电极产品由植入式脊髓神经刺激电极、电极固定锚、造隧道工具、导丝、穿刺针、钢丝、力矩螺丝刀及备用的电极固定锚组成。植入式脊髓神经刺激延伸导线由延伸导线、套筒、备份螺钉、造隧道工具、力矩螺丝刀组成。上述产品与适配的植入式脊髓神经刺激器配合使用,供18周岁及以上患者使用(孕妇除外),用于躯干、四肢的慢性顽固性疼痛的辅助治疗。
植入式脊髓神经刺激电极和植入式脊髓神经刺激延伸导线主要采用高密度连接和抗弯曲疲劳核心技术,使用新型夹芯电极固定锚,可增强对电极的固定力,降低电极移位率。属于国内首创医疗器械。
(三)神经外科手术导航定位系统:该产品由红外摄像机、工作站、支架、定位组件(探针、参考架、连接器、反光球、手术器械适配器)、激光探针、手持激光瞄准器、脚踏开关、自动定位装置组成。用于神经外科手术器械和植入物的导航和定向定位。
该产品主要采用多模态影像融合、激光面注册、自动定位装置等核心技术,具备自动定位装置,属于具有自主知识产权的国内首创医疗器械,各项性能指标达到国际同品种器械水平。该产品可以在保证定位精度的基础上,提高手术效率,并且能实现机械臂的基本功能。
(四)直管型胸主动脉覆膜支架系统:该产品由自膨胀的覆膜支架和输送系统构成。覆膜支架由聚酯膜通过聚酯缝合线与多段自扩张的镍钛合金支架段缝合而成。覆膜支架的远端为有孔覆膜设计,用以撑开主动脉真腔,利于主动脉的重塑。同时,可以保持远端分支血管的通畅,以降低术后脊髓缺血导致的截瘫发生率。另外大锥度的覆膜支架设计能更好的顺应人体血管渐细的形态。该产品的输送系统由锥形头、内管、外管、手柄等零部件组成,用于实现覆膜支架在人体内的导入和释放。输送系统的低外径降低了系统入路血管直径要求,使得支架更加容易推送至病变血管位置,减少了手术创伤以及因下肢缺血风险带来的并发症。
该产品用于治疗Stanford B型主动脉夹层的患者,预期让更多的主动脉夹层患者受益。
(五)双通道植入式脑深部电刺激脉冲发生器套件、植入式脑深部电刺激电极导线套件和植入式脑深部电刺激延伸导线套件设备:2个双通道植入式脑深部电刺激脉冲发生器套件由脉冲发生器、力矩螺丝刀和封堵头组成,其中一个产品具有充电功能,产品名称为双通道可充电植入式脑深部电刺激脉冲发生器套件。
植入式脑深部电刺激电极导线套件由电极、电极固定组件、限深器、电极保护帽组件、简易电极保护帽、短导丝部件、电极造隧道工具、自锁测试电缆、鳄鱼夹测试电缆、力矩螺丝刀和电极固定装置(视不同型号选择)及备用选配件电极固定组件(型号:A6026)、电极保护帽组件(型号:A6023)、简易电极保护帽(型号:A6024)、短导丝部件(型号:A6025)、电极固定装置(型号:LF01)组成。
植入式脑深部电刺激延伸导线套件由延伸导线套件及备用选配件金属网连接套筒、造隧道工具组成。
脉冲发生器套件、电极导线套件和延伸导线套件产品需配合使用,产生电刺激脉冲,对丘脑底核(STN)进行刺激,用于对药物不能有效控制某些症状的晚期左旋多巴反应性帕金森病患者的联合治疗。
上述产品具有抗干扰设计,可接受3.0T场强磁共振成像检查,具有完备的自主知识产权,属于国内首创医疗器械。电极导线套件和延伸导线套件产品采用一种包覆于电极导线上的编织复合导电屏蔽结构的制造技术,可显著降低射频场造成的温升。植入该类产品的患者不但能在1.5T MRI设备下安全地进行磁共振扫描,而且能在3.0T MRI设备下进行扫描,进而获得高质量的MRI影像资料。
(六)腹腔内窥镜手术系统设备:该产品由医生控制台、患者手术平台、图像平台、三维电子内窥镜、内窥镜图像处理器、无源手术器械、高频手术器械和附件组成。由医师利用主从操控系统对于微创手术器械进行控制,用于泌尿外科腹腔镜手术操作。
该产品主要采用微型精度高手术器械,能提高术中主从操作的精度和顺畅度;采用位姿解耦的自平衡主手构型设计,可缩短学习曲线、提升操作直观性;采用三维电子高清视觉系统,能提供立体、直观、清晰的手术信息;具备力感告警安全机制能保证手术安全,消除术中非预期运动。该产品具有完整自主知识产权。
该产品能提高手术质量,保证操作的安全性,与进口产品相比,将大幅降低治疗费用,减轻患者经济负担。
(七)消化道振动胶囊系统:该产品由一次性使用消化道振动胶囊(简称胶囊)、配置器和VCP软件(VCP2.1)组成,适用于药物治疗效果欠佳的成人功能性慢性传输型便秘的症状缓解,在医疗机构中经有资质医师指导下使用。
本产品通过振动对结肠壁进行刺激,促进结肠蠕动,为药物治疗效果欠佳的成人功能性慢性传输型便秘提供了一种全新治疗办法。该产品为同类首个,目前国内外尚无同类产品上市。本产品创新点:一是胶囊具备加速度检测能力,可以通过监测加速度数值的变化情况进而启动胶囊;二是产品属于非药物治疗,可作为功能性便秘人群的另一种治疗方案。
目前便秘治疗虽然有多种方法可供选择,但存在患病率高、治疗副作用、复发率高和病人满意度低的情况。本产品预期可提升适用人群的生活质量。
(八)移动式头颈磁共振成像系统:该产品由永磁磁体、梯度放大器、梯度匀场线圈、射频放大器、射频发射线圈、头线圈(可选)、头颈联合线圈(可选)、谱仪、温度控制器、数字匀场单元、移动装置、屏蔽罩、病床、报警单元组成,供头部、颈部临床MRI诊断。
该产品具有可移动、体积小、重量轻、一体化结构的特点。可部署于固定屏蔽室外的医疗机构内部,外接220V AC/10A网电源使用;也可移动至医疗机构的不同场地,对患者进行抵近检查,扩大了磁共振产品的安装范围。
(九)颅内出血CT影像辅助分诊软件:该产品由服务器端及浏览器端构成。服务器端由数据访问和存储模块、数据同步模块和基于深度学习算法的图像处理模块组成;浏览器端由患者管理模块、结果显示和编辑模块、服务模块组成。软件通过FTP下载的方式交付。
该产品为国内首款基于深度学习技术实现颅内出血分诊提示以及测量分析的人工智能医疗软件,采用基于深度学习的颅内出血检出与分割算法,实现颅内出血分诊提示和出血体积定量分析功能,可对颅脑CT平扫影像进行显示、处理、测量和分析,用于对超急性期、急性期颅内出血患者的分诊提示。临床供经培训合格的医师使用,不能单独作为临床诊疗决策的依据。
该产品创新性地使用人工智能算法对患者图像即时进行计算和分析,提高诊断速度,快速筛选出超急性期和急性期疑似颅内出血患者,为医生评估危急程度、制定临床方案提供参考依据,有效的帮助患者尽早诊断和救治。
(十)磁共振成像系统:该产品由超导磁体(1.5T)、扫描床、谱仪、射频系统、梯度系统、操作台、隔离变压器、发射线圈、梯度线圈、呼吸门控、射频接收线圈组成,供临床MRI图像诊断。
该产品的主要创新点为采用了无液氦超导磁体技术,该超导磁体采用制冷机直接传导冷却。与常规使用液氦对磁体中的超导线圈进行冷却的超导磁共振产品相比,该产品生产使用的成本更低,可简化磁体结构,减轻磁体重量等优势。目前该产品的2项关键技术已在中国申请发明专利,并进入了实质审查阶段。
(十一)髋关节置换手术导航定位系统:该产品由机械臂系统、光学定位系统、导航控制系统、术前规划软件、脚踏开关、加密装置、附件组成。仅与经验证的髋关节假体和手术工具联合使用,在成人髋关节置换手术过程中用于手术工具和髋关节假体的导航定位。
该产品核心技术主要包括空间配准、机械臂控制、安全边界控制等技术。在髋关节置换手术中应用其自由度机械臂作业并具有安全边界控制功能,辅助医生完成髋臼打磨、股骨截骨、髋关节假体安装等工作,与传统人工髋关节置换术相比,可以保证手术定位精度,减轻不良事件和并发症的发生概率,降低X射线对医生和患者的辐射损伤。
该产品属于具有自主知识产权的国内首创医疗器械,各项性能指标达到国际同品种器械水平。
(十二)膝关节置换手术导航定位系统:该产品由导航控制台(导航台车、光学导航设备、显示器)、手术平台(机械臂、手术台车)、手术辅助工具、光学定位标记、脚踏开关和线缆组成。与经验证的膝关节假体联合使用,在成人全膝关节置换手术中,用于膝关节假体和手术工具的导航定位。
该产品核心技术包括导航引导下机器人截骨定位技术和多裕度的安全保护机制。在全膝关节置换手术中应用6自由度机械臂握持接骨板,与传统膝关节置换手术相比,可减少患者创伤,手术导航定位精度满足临床使用要求,降低X射线对患者和医生的辐射损伤。
该产品属于具有自主知识产权的国内首创医疗器械,各项性能指标达到国际同品种器械水平。
(十三)脊髓神经刺激测试电极:该产品由电极、导丝、穿刺针、钢丝组成。与适配的体外测试刺激器、程控仪和多电极测试电缆配合使用,用于评估脊髓神经刺激系统对于躯干、四肢的慢性顽固性疼痛的治疗效果。
该产品可以根据患者姿势自动调用预设置的刺激参数,使患者达到当前满意的治疗状态。并支持远程程控功能,提供了一种患者不必到医院就能实现参数调整的方法,可减少患者往返医院的次数。
(十四)膝关节置换手术导航定位系统:该产品由机械臂系统、导航仪系统、主控台车系统、手术电动工具组成。与经验证的膝关节假体及定位工具联合使用,在成人全膝关节置换手术中,用于膝关节假体和手术工具的导航定位。
该产品核心技术包括注册配准算法、导航截骨安全控制算法、以及机械臂术中运动追踪算法等。在全膝关节置换手术中采用齿轮驱动的七自由度机械臂系统握持手术电动工具,可辅助医生完成全膝关节置换手术,手术导航定位精度满足临床使用要求,降低X射线对医生和患者的辐射损伤。
该产品属于具有自主知识产权的国内首创医疗器械,各项性能指标达到国际同品种器械水平。
(十五)髂静脉支架系统:该产品由髂静脉支架和输送系统组成。髂静脉支架由镍钛合金制成。输送系统由输送鞘组件、推杆组件、尖端和手柄等部件组成。该产品在髂总静脉内使用,用于治疗非血栓性髂静脉压迫综合征。
该产品的特殊设计可以减少支架对侧髂静脉血液回流的影响,提高支架的定位及释放的准确性,更好解决髂静脉受压问题及增加产品柔顺性。该产品的上市为临床髂静脉疾病介入治疗提供了新的选择。
(十六)经导管植入式无导线起搏系统:该系统由植入式脉冲发生器(含固定翼)和输送导管组成。可在右心室内感知患者心脏活动,监测心动过缓心律并针对心动过缓提供起搏治疗。该系统为磁共振环境条件安全的医疗器械,在规定的条件及保证对患者和植入设备采取了特殊保护措施的前提下,患者可接受临床1.5T和3.0T场强的磁共振成像检查。
与传统起搏器相比,该系统只需在心室中植入单个脉冲发生器即可提供房室同步起搏,不需要放置心脏起搏器的皮下囊袋和经静脉连接到心房、心室的导线,可减少囊袋和电极导线相关的并发症。在使用该系统时,因无需将起搏器电极导线穿过静脉或三尖瓣,使得静脉阻塞的患者也可以植入起搏器。
该系统在前代产品的基础上增加了机械感知和房室同步起搏技术,利用内置三轴加速计在心室内感知心房机械信号,实现房室同步起搏,与已有的VVI单心室起搏模式相比,房室同步起搏可以增加心室中的血液量,使得每次心室搏动时的每搏输出量增加,从而带来相应的临床获益。
该系统采用的无导线起搏器中的机械感知和房室同步起搏技术,在国内外均为首创。
(十七)血管内成像设备:血管内成像设备由主机、探头接口单元(PIU)、推车组件和显示器组成。该设备与一次性使用血管内成像导管连接配合使用,用于在进行经皮冠状动脉介入手术时对冠状动脉进行血管内成像。设备利用PIU控制成像导管驱动探头360°旋转和回撤,由成像段完成对血管的扫描。同时,设备发射近红外光和超声波,干涉仪和超声模块记录不同深度血管的反射光和超声发射,主机重建反射光信号和超声反射信号,形成血管内超声图像和血管内光学干涉断层图像。
该设备在产品设计上,设计了同步电路,能够通过探测血管内超声(IVUS)探头和血管内光相干断层成像(OCT)探头的位置关系,使用校正算法,实现两种图像的配准,实现了同步成像。该设备将IVUS和OCT两种功能进行整合,与已上市且只有单功能成像产品相比,能同时同步实现上述两种成像。满足医生对分辨率和穿透力的要求。快速成像后还可以按照临床医生需求的速度回放图像,为医生诊断提供更多信息。
(十八)一次性使用血管内成像导管:一次性使用血管内成像导管由外鞘管、成像轴、压力延长管和三通连接件组成。其中外鞘管包括接头、接头保护帽、冲洗口、回拉管、行程管、近端鞘管、远端鞘管、快速交换头和显影环,成像轴包括接头、扭矩弹簧和探头。C1-1型中的探头为超声探头和光学探头;C2-1型中的探头为超声探头;C3-1型中的探头为光学探头。
该产品在设计上,通过微型化设计和显微制造,缩小探头尺寸,将光学探头和超声探头前后排列,采用光纤和电导线与其连接,保证了导管整体粗细基本不变。此外,该产品将血管内超声(IVUS)和血管内光相干断层成像(OCT)两种功能进行了整合,与已上市且只有单功能成像产品相比,能同时同步实现上述两种成像,不仅发挥两种技术的优势,还简化了医生操作,提高了成像的准确性和安全性。满足医生对分辨和穿透力的要求。快速成像后还可以按照临床医生需求的速度回放图像,为医生诊断提供更多信息。
(十九)患者程控充电器:该产品由电源适配器、充电控制器、充电线圈和充电腰带组件组成。供18周岁及以上患者使用(孕妇除外),用于对适配的可充电植入式脊髓神经刺激器进行充电、程控。
该产品核心技术为近场/蓝牙双备份安全通信技术、远程程控技术和无线充电技术。可直接与脉冲发生器建立蓝牙连接,提高患者接收程控的使用体验。产品具有近场和蓝牙两种安全通信技术,一种通信方式故障时,可启用另一种通信方式。蓝牙通信平时默认关闭,避免误连接其他蓝牙设备导致设备故障或参数变化,患者需要程控时,可通过近场通信唤醒蓝牙通信程控功能。
该产品属于脊髓神经刺激系统的一部分,脊髓神经刺激系统可为患者提供更多的治疗选择,根据患者姿势自动调用预参数,更精细化的实现远程程控功能,该功能提供了一种患者不必到医院就实现参数调整的方法,能减少患者往返医院次数。
(二十)胸主动脉支架系统:该产品由近端胸主动脉覆膜支架系统和远端胸主动脉裸支架系统组成。近端胸主动脉覆膜支架系统封堵B型夹层近端破口,促使假腔内血栓化;远端胸主动脉裸支架系统扩张降主动脉远端真腔,促进主动脉真腔重塑。其中支架的结构设计使其具有良好的柔顺性及一定的径向和轴向支撑力。胸主动脉覆膜支架和胸主动脉裸支架分别预装在对应的输送器中,输送器的设计可保证释放过程的稳定性及支架精准定位。
主动脉夹层起病急,进展快,病死率高,支架类产品已成为腔内介入治疗该类疾病的主要手段。该产品适用于治疗Stanford B型夹层,支架近端锚定区长度≥15mm,且病变符合以下条件之一:1.存在远端破口,有处理远端病变的必要性;2.夹层累及范围较广,且存在远端真腔塌陷;3.夹层伴远端灌注不良。该产品的上市将为患者带来新的治疗选择。
(二十一)消化道内窥镜用超声诊断设备:该产品由超声探头、探头驱动器、图像处理器、键盘和脚踏开关组成。与独立供电的显示器配合使用,用于对人体消化道(包括食管、胃、十二指肠和结肠)及周边组织进行超声成像。
该产品为配合消化道内窥镜使用的超声诊断设备。使用时超声探头通过消化道内窥镜的工作通道进入人体消化道内,超声图像处理器输出控制信号,由探头驱动器驱动超声探头里的软轴旋转,带动前端单阵元超声换能器进行机械环扫,向检查部位发射超声脉冲,获得超声回波信号后, 超声图像处理器对信号处理,可在显示器上呈现二维黑白图像,用于超声诊断检查。
该产品超声探头回波信号灵敏度提高了20%,相对带宽达到40%。在保证探头空间尺寸的基础上增大回波信号,增强了微弱组织信号,能保证单一接收成像精度,加大了2种频率的超声探头(12MHz、20MHz)探测深度和分辨力。
临床上该产品主要用于消化道及周边组织黏膜下早期病变的超声诊断(肿瘤浸润深度、有无周围淋巴结及邻近器官转移),是国内首次将超声影像技术应用于下消化道领域,可在常规内窥镜检查的基础上对更深层次的组织进行成像检查,对于直径<2cm的消化道黏膜下病变具有临床优势。
(二十二)一次性使用冷冻消融球囊导管:该产品由球囊、导管主体(真空外管、真空内管、回气管、进气管、缓冲管、保护管)和手柄(手柄座、回路连接管、真空连接管、接头)组成。与特定的冷冻消融设备配合使用,用于T1期非肌层浸润性膀胱癌(NMIBC)成人患者在首次经尿道膀胱肿瘤电切术(TURBt)后进行冷冻消融的辅助治疗。
目前国内尚无膀胱肿瘤冷冻类医疗器械,国产探针型冷冻医疗器械产品仅限于实体肿瘤的应用,进口球囊型冷冻医疗器械产品仅限于心血管系统的应用。该产品核心技术为导管头端采用创新的球囊结构设计,球囊远端内凹,可实现球囊侧面和远端的有效冷冻。球囊远端还设计了缓冲单元,可增加产品安全性,有助于导管的输送。该产品拥有自主知识产权,工作原理为国内首创。
(二十三)腹腔内窥镜手术系统:该产品由医生控制台、患者手术台、手术器械和附件组成。由医师利用主从操控系统对微创手术进行控制,用于泌尿外科上尿路腹腔镜手术。
该产品医生控制台是腹腔内窥镜手术系统的核心部分,医生通过两个主手控制器和脚踏板装置控制3D内窥镜和手术器械实现对患者的手术操作。患者手术平台是腹腔内窥镜手术系统的操作部分,主要功能是支撑手术器械和腹腔镜设备。随着医生控制台主手控制器和脚踏装置的操作,机械臂系统做出相应的操作,每条机械臂的关节处具有多个活动自由度,可提高手术的灵活性和精度,滤除人手自然颤动。手术器械协助完成手术切割、缝合、夹取等工作。
该产品具有自主知识产权,与传统的腹腔镜手术相比,该产品能提高手术质量,保证操作的安全性。与进口产品相比,能降低治疗费用,减轻患者经济负担。
(二十四)经导管人工肺动脉瓣膜系统:该产品由肺动脉瓣膜和输送系统组成,其中输送系统包括输送导管系统和压缩装载系统。肺动脉瓣膜由自扩张镍钛合金支架、猪心包材质的瓣叶和裙体及缝合线组成。肺动脉瓣膜的设计能够使瓣膜支架锚定更加稳定,适用于不同解剖形态的肺动脉瓣环范围更大的患者,同时使支架输送更安全,血液流动更顺畅。输送系统的设计使瓣膜可被均匀一致地压缩,提高了装载效率,降低了瓣膜释放时径向折叠风险。
该产品适用于严重肺动脉瓣反流(≥3+)的有自体右心室流出道的先心病术后患者(年龄≥12岁,体重≥30kg),且需符合一定的临床使用条件(详见产品适用范围)。产品的上市将为患者带来新的治疗选择。
(二十五)植入式左心室辅助系统:该产品由植入部件(血泵、心室缝合环、人造血管保护架)、手术工具(心脏开孔工具、旋紧工具、经皮导线牵引工具、入口管保护帽、手术用经皮导线延长线)、体外部件(控制器、控制器电源延长线、交流电源适配器、锂离子电池、电池充电器、监控器(选配)、监控器数据线(选配)、患者背包和淋浴包)组成。
该产品与特定人工血管配套使用,为进展期难治性左心衰患者血液循环提供机械支持,用于心脏移植前或恢复心脏功能的过渡治疗。供具备心脏移植条件与术后综合护理能力的医疗机构使用,医务人员、院外护理人员及患者须通过相应培训。抗凝治疗不耐受患者禁用。
该产品采用泵机一体化设计、磁液悬浮、内流道优化、驱动双冗余等主要核心技术,均拥有自主知识产权,是国内首个采用磁液悬浮技术的植入式磁液悬浮左心室辅助系统,其关键技术指标已达到国际同等水平。
对于患有终末期心力衰竭且面临死亡风险患者的短期辅助、过渡到恢复和过渡到移植的治疗将发挥重要作用。
(二十六)伽玛射束立体定向放射治疗系统:该产品由主机系统、电气控制系统、放射治疗计划系统软件、治疗控制系统软件、图像引导系统和射野验证系统组成。用于对实体肿瘤和病变进行图像引导的头部立体定向放射治疗、放射外科治疗和体部立体定向放射治疗。
该产品融合了KV级CBCT图像引导技术和实时正交成像图像引导技术,具有自主知识产权,是国内首创的影像引导伽玛射线立体定向放射治疗设备。产品采用滚筒结构设计,在滚筒上安装有KV级X射线图像引导模块和MV级的EPID模块,与聚焦治疗头在结构布局上同轴共面,可实现基于CBCT成像技术和正交成像技术的图像引导摆位验证及基于正交成像技术的实时图像引导。
该产品在治疗前可对患者进行基于CBCT成像技术和正交成像技术的图像引导摆位验证,通过影像系统检测患者治疗前的摆位偏差并通知控制系统进行必要的位置调整,确保将正确的计划治疗靶区送入治疗区域;在治疗过程中可进行基于正交成像技术的实时图像引导,实时图像引导技术可实时监控患者体位的变化,对超出临床可接受范围的患者位置误差实时进行调整,确保放射治疗的靶区位置精度,提高放射治疗的临床疗效,避免正常组织接受不必要的照射,保证患者治疗时的位置精度。
此外,该产品基于EPID的射野验证系统,优化了日常质控工作流程,可在日常质控过程中用于测量准直器输出射野的大小和位置,验证准直器位置精度,保证照射剂量的准确性,提高产品可靠性,为精准治疗提供基础保障。
(二十七)耳鼻喉双源锥形束计算机体层摄影设备:该产品由大视野成像系统、小视野成像系统、控制装置、扫描床、头托、机架、激光定位灯、工作站组成。用于耳部、鼻部、咽喉部气道、口腔颌面部的X射线锥形束体层摄影检查。
该产品是全球首款双源、双探测器的口腔CBCT产品,其核心技术为双源成像技术,采用小焦点、高功率X射线管头和高分辨率探测器提升了空间分辨率,在满足口腔颌面部成像需求的基础上,能够为耳鼻喉科疾病提供X射线锥形束体层摄影检查。其大视野成像系统用于口腔颌面部、鼻部和咽喉部气道的常规成像检查,小视野成像系统具有高空间分辨率,用于耳部内部机构(中耳、内耳)的成像检查。
(二十八)血管内超声诊断仪和一次性使用血管内超声诊断导管:血管内超声诊断仪由成像主机(含推车、显示器、键盘、鼠标)和回撤马达组成。一次性使用血管内超声诊断导管由血管内超声诊断导管和配套附件组成,其中血管内超声诊断导管由外鞘管和成像信号传输组件构成,附件包括延长管、注射器(3mL和10mL)和三通阀。血管内超声诊断仪和一次性使用血管内超声诊断导管配合使用,适用于将进行冠脉血管内介入手术的患者对冠脉血管的超声检查。
血管内超声诊断仪和一次性使用血管内超声诊断导管配合使用,利用超声脉冲回波原理对血管进行新型高速三维机械扫描成像。诊断仪发射电脉冲激励导管前端的超声换能器产生超声波,通过血管壁内侧反射后经超声换能器接收转换成电信号并传输给诊断仪,经过处理后以二维灰度图像方式显示在主机的显示器上,以反映血管内部结构特征,供医生进行临床诊断。
血管内超声诊断仪和一次性使用血管内超声诊断导管配合使用中,利用导管技术将微型超声探头送入冠脉血管腔中,对血管结构进行超声成像,可识别斑块、夹层、血栓、支架和导丝等血管腔内组织和器械,并实施各种参数的定量测量,可为冠脉介入手术提供更精准的术前策略指导和术后效果评价,其采用了两种超声频率,具有有较高的回撤速度、较长的最大回撤距离和较快的旋转扫描速度。基于上述特点,该产品针对弥漫性病变,一次回撤即可完成扫描,可减少手术步骤和手术时间。
(二十九)肠息肉电子结肠内窥镜图像辅助检测软件:该产品以光盘形式提供,以单机方式安装使用。具有采集卡管理、授权管理、绘制检测区域、声音提示、显示选项、显示软件信息、监测运行时间、处理算法管理、主程序9大功能模块。产品仅在医疗机构内与指定型号的电子结肠内窥镜配合使用,供执业医生在成人结肠内窥镜检查时,对输出的独立视频图像进行实时显示疑似息肉区域。该信息仅供参考,医生应当结合患者病情进行临床决策。
该产品工作原理为在内窥镜图像处理器的视频信号输出端口导入视频图像,经过软件处理和算法分析后找出其中疑似息肉的位置,并在单独的显示器中显示。该产品为国内首个利用深度学习技术对内窥镜图像中息肉进行辅助检测的医疗器械软件,采用了小样本深度学习技术和局部标记技术进行算法模型框架的选择和开发,算法的整体性能不完全依赖训练数据的增加,能够在较小样本下实现高性能、强泛化性和鲁棒性。
该产品与电子结肠内窥镜配合使用,可帮助医生在进行结肠镜检查时找出疑似息肉位置,有利于更早发现直肠癌的癌前病变,从而降低直肠癌发生率和死亡率。
(三十)可吸收再生氧化纤维素止血颗粒:该产品由型号3013SP即再生氧化纤维素可吸收止血颗粒(预装含装置)和型号3123SPEA 即再生氧化纤维素可吸收止血颗粒内窥镜施用导管装置组成。两者均经辐射灭菌,一次性使用。型号3013SP为预装3g经专利工艺压实细纤维制成的止血颗粒的施用装置,用于开放手术;型号 3123SPEA,可配合3013SP用于内窥镜手术。
该产品适用于外科手术或内窥镜手术中(眼科、神经外科、泌尿外科除外),结扎法或其他传统控制方法不适用或无效时,作为辅助控制毛细血管、小静脉和小动脉出血。该产品为首个颗粒状的再生氧化纤维素止血产品,其颗粒由专利工艺压实细纤维制成,其配套用的施粉装置可以使器械朝向不影响颗粒的有效均匀喷射,便于外科手术或内窥镜手术中的应用。
(三十一)脑炎/脑膜炎多重病原体核酸联合检测试剂盒(封闭巢式多重PCR熔解曲线法):该产品由FilmArray ME测试条、样本缓冲液、溶解液、一次性使用红色样本注射管和独立包装移液管组成,是一种一次性封闭检测试剂,用于体外定性检测具有脑膜炎及/或脑炎体征及/或症状的人群的脑脊液 (CSF)样本中的14 种细菌、病毒和隐形球菌的核酸。
该产品采用封闭巢式多重PCR熔解曲线法,基于多重巢式 PCR 扩增和熔解曲线分析技术,对经机械研磨破碎后的样本进行检测分析。多重巢式 PCR 扩增结合熔解曲线分析技术提高了检测试剂盒的反应灵敏度和特异性,系统软件自动评估数据并报告结果。
该产品检测鉴定CSF中14 种潜在中枢神经系统感染相关病原体,可在1小时左右获得检测结果,加快了脑炎脑膜炎的病原学诊断,从而可尽早开展针对性的临床治疗,降低了脑炎脑膜炎等疾病给患者带来的负担。
(三十二)吻合口加固修补片:吻合口加固修补片共包含管状型、平片型、圆型。管状型和圆型由修补片、背衬、牵引线三部分构成,平片型只有修补片。修补片由脱细胞猪小肠粘膜下层材料制备而成,与背衬用牵引线进行缝合固定。平片型无背衬和牵引线。
该产品是可降解吻合口加固产品,其采用的生产工艺实现了去除动物组织免疫原性的同时,保留天然细胞外基质的结构和生物活性;其结构设计使产品能配套连接各种型号吻合器并提高手术安全性。该产品配合吻合器用于吻合部位的加固,适用于远端胃切除术、近端胃切除术、袖状胃切除术、胃肠吻合术,能够降低胃肠切除手术术后发生吻合口漏、出血等相关并发症,为患者带来受益。
(三十三)医用粘合剂:由人血白蛋白溶液、琥珀酰亚胺琥珀酸酯-聚乙二醇-琥珀酰亚胺琥珀酸酯(简称: SS-PEG-SS)、无菌溶剂、一次性使用无菌双联混药包4个部件组成。产品所用人血白蛋白溶液以市售药品级20%人血白蛋白为原料,在其中加入少量磷酸二氢钠-碳酸钠缓冲盐调节pH,分装后经电子束辐照灭菌。SS-PEG-SS为万级车间生产产品,分子量约为4000D,分装后经电子束辐照灭菌。无菌溶剂成分为水,经湿热灭菌。一次性使用无菌双联混药包经环氧乙烷灭菌。
肺实质切除术中,用标准缝合/钉合法等常规方法闭合创面后,浸没式气漏测试法观察脏层胸膜仍存在2级漏气时,可在闭合后的脏层胸膜漏气部位使用本产品进行辅助封合。该产品是国内首个用于封合肺实质漏气的粘合剂医疗器械。
(三十四)慢性青光眼样视神经病变眼底图像辅助诊断软件:该产品由服务器端、管理平台和临床客户端组成,包括图像基本操作、检查管理和基于深度学习技术的病变风险判断3个功能模块。该产品在医疗机构与特定型号的眼底照相机配合使用,用于需要进行眼底照相以判断是否具有相关疾病或存在相关疾病风险的成年患者,检测结果仅为执业医师提供可疑慢性青光眼样视神经病变的提示和是否需进一步就医检查的辅助诊断建议。不适用于高度近视人群。
该产品为医用人工智能独立软件,采用深度学习的人工智能算法提供临床辅助分诊建议。产品基于不同视野范围,分别构建了对应的子分类模型,算法引擎采用多模型集成学习策略,给出有无疑似慢性青光眼样视神经病变的提示,供专业医生参考。
该产品提供了一种质控方法,能够自动识别非眼底图像、大面积污损和屈光间质浑浊等临床中常见的眼底图像质量问题,有效提升了辅助诊断的准确率和置信度,有望解决我国青光眼诊断面临的医疗资源不足的问题。
(三十五)磁共振成像系统:该产品由超导磁体(5.0T)、梯度功率放大器、梯度线圈、射频功率放大器、射频线圈、检查床、谱仪、配电系统、对讲系统和生理信号门控单元组成。适用于体重大于20 kg患者的临床MRI诊断。
该产品采用全身临床5.0T超导磁体,首次在超高场磁共振系统中将全身体激发线圈应用于临床扫描,从而实现全身成像,可以提升图像信噪比和图像空间分辨率,并实现超高场体部成像。
该产品核心技术为全身临床 5.0T 超导磁体、多通道射频并行发射控制和超高场磁共振系统射频安全成像,均拥有自主知识产权,关键性能指标已达到国际领先水平。
(三十六)优美莫司涂层冠状动脉球囊扩张导管:优美莫司涂层冠状动脉球囊扩张导管由球囊扩张导管及球囊上的药物涂层组成,球囊导管由球囊、远端管、过渡管和近端管等组成。药物涂层含有优美莫司和聚环氧乙烷载体,药物剂量为3μg/mm2。产品经环氧乙烷灭菌,一次性使用。该产品通过聚环氧乙烷载体将优美莫司药物粘附在球囊表面,聚环氧乙烷的亲水特性和优美莫司的亲脂特性使药物可以从球囊表面释放并快速进入血管壁。
药物球囊作为一种血管内药物释放技术,能在病变部位释放有效治疗浓度的药物,解决并治疗冠心病介入及支架内再狭窄病变。该产品适用于血管直径2.0mm-2.75mm原发冠状动脉血管病变治疗,为原发小血管病变患者提供了新的选择。
(三十七)质子治疗系统:该产品是国内首个获批上市的质子治疗系统。由加速器系统和治疗系统两部分组成。其中加速器系统包括注入器系统、低能传输系统、主加速器系统、高能束流传输系统和辅助电气系统,治疗系统包括固定束治疗系统、180°旋转束治疗系统和治疗计划系统。产品提供质子束进行放射治疗,在实现肿瘤部位高剂量的同时,可降低周围正常组织剂量,特别是靶区后组织的剂量,适用于治疗全身实体恶性肿瘤和某些良性疾病,具体适应症应由临床医师根据实际情况确定。
(三十八)集成膜式氧合器:集成膜式氧合器由氧合器组件(集成气体交换器和热交换器)和静脉贮血器系统组成,可组合使用,氧合器组件集成动脉微栓过滤功能(可选)。该产品适用于体重>10kg的患者。氧合器适用于体外循环手术(时间不超过6小时)中血液的氧合和二氧化碳的排除,并调节血液温度。静脉贮血器系统用于收集、存储和过滤血液。
该产品采用了螺旋导流集成化结构,在血液入口处通过螺旋导流结构引导血液快速分散流动,在进入变温室进行气体交换时,通过由内到外的多孔状导流结构,实现血液的二次分流,使血液在整个氧合器腔体内均匀的分布,缩短血流路径,提升氧合器的气体交换能力同时降低压力损失。在临床应用中集成的结构设计具有可减少整体预充量,减少血液稀释的临床意义。
(三十九)颅内动脉瘤手术计划软件:该产品由应用程序和授权文件组成,软件功能模块包括数据加载、显示交互、数据管理、数据处理和日志。产品用于脑血管病患者X射线血管造影三维体层图像的显示、分割、测量和处理,辅助医生在神经介入手术时进行动脉瘤弹簧圈栓塞用的微导管路径和塑形规划。
该产品利用医学图像处理技术对颅内动脉瘤患者的X射线血管造影三维体层图像进行处理,实现三维血管重建、动脉瘤分割和自动测量及微导管路径和塑形针形状规划,帮助医生进行术前方案规划。与传统神经介入手术方式相比,该产品可以提升微导管一次性到位率,缩短微导管输送时间,降低术中微导管反复推送对血管刺激导致的并发症发生概率,减少医生、患者X射线辐射时间。
(四十)血流导向密网支架:血流导向密网支架的植入物为柱形自扩张支架,由自膨胀式钴铬合金和铂钨合金丝编织而成。输送系统由推送杆、不锈钢线圈、漏斗、支撑垫、编织管、标记环、铂金线圈、警告标记、热缩管、粘接剂组成。该产品的创新点在于利用输送系统中的机械球囊,从支架内部进行主动辅助膨胀,将支架推送到治疗部位,并且在需要时实现对支架的回收。
该产品用于成人患者颈内动脉(岩骨段至末端)与椎动脉未破裂的囊状或梭状的宽颈(瘤颈宽≥4mm或瘤体/瘤颈比<2)动脉瘤,且载瘤血管直径≥2.0mm且≤5.6mm。产品的上市将为患者带来新的治疗选择。
(四十一)非球面衍射型多焦人工晶状体:非球面衍射型多焦人工晶状体为一件式/后房人工晶状体,可折叠,襻形为改良L型。该产品主体及支撑部分均由丙烯酸乙酯、甲基丙烯酸乙酯共聚物材料制成,添加了紫外线吸收剂,表面经肝素改性。该产品的创新点在于其光学部采用衍射分光和非球面相结合的设计,衍射技术是实现多焦点的核心,在国内属于首创。
该产品用于成年白内障患者的视力矫正,预期可提供远、近两个焦点,一定程度上弥补了单焦点人工晶状体视力不佳的不足。产品的上市将为患者带来新的治疗选择。
(四十二)左心耳封堵器系统:左心耳封堵器系统由左心耳封堵器和输送器组成,其中左心耳封堵器由密封盘和锚定盘连接而成。输送器由输送鞘管、扩张器、装载器、输送钢缆和止血阀组成。该产品的密封盘和锚定盘的设计均采用了创新的专利设计,充分利用了镍钛丝编织结构的自适应性,一定程度上可满足临床对不同形态左心耳的封堵需求。
该产品适用于有卒中风险(CHA2DS2-VASc评分≥2分)且长期口服抗凝治疗禁忌的非瓣膜性房颤患者。产品的上市预期让更多的患者受益。
(四十三)人工血管:人工血管主要由PET线编织制成,涂覆有牛胶原蛋白和甘油。该产品的聚酯编织采用创新编制工艺,外层经纱采用弹性纱线(涤纶低弹丝DTY纱线),中间层采用非弹性纱线(涤纶全牵伸FDY纱线),纬纱采用弹性纱线、非弹性纱线组成的复合纱线。该编制工艺使织物具有更小且更均匀的孔隙,预期将改进成品的渗血性能。人工血管用于主动脉及其分支血管的置换或旁路手术。该产品的上市将为临床治疗提供更多选择。
(四十四)一次性使用压力监测磁定位射频消融导管:该产品由射频消融导管、连接尾线和尾线连接盒组成。其中导管主体包含高扭矩管身和可弯曲的头部,头部装有铂铱电极,1个头端电极和3个环形电极。该产品在医疗机构中与上海微创电生理医疗科技股份有限公司生产的三维心脏电生理标测系统和心脏射频消融仪配合使用,用于药物难治性、复发性、症状性阵发性房颤的治疗。
该产品采用了基于应变片原理压力传感技术、磁场定位技术、头端多孔盐水灌注技术与三维电生理标测系统,可为房颤患者的治疗提供整体解决方案,是国产首个具有压力感知功能的心脏射频消融导管。与传统心脏类射频消融导管相比,该产品可以实时测量导管头端和心壁之间触点压力值,更好的辅助术者完成手术,有效防止术中导管与组织贴靠力过大造成蒸汽爆裂或过小引起消融不完全,可缩短医生学习曲线,达到更优的远期治疗成功率。
(四十五)血管内超声诊断设备与一次性使用血管内超声诊断导管:该配套产品利用脉冲回波原理对血管进行超声扫描成像。设备主机和导管控制器向位于导管远端的超声换能器发出激励脉冲,同时通过导管鞘管内部的驱动轴带动换能器高速旋转,换能器发出超声波脉冲并接受血管组织反射的超声回波信号,经导管控制器放大、采集、预处理后传输至主机,实现血管图像的显示和处理。
血管内超声诊断设备采用全数字信号传输、单阵元机械旋转式设计,导管控制器与成像主机之间实现了数字传输,提高了系统的集成度和稳定性的同时降低了成本,使图像噪声更小。
一次性使用血管内超声诊断导管,在PMN-PT高频单晶复合材料换能器上,采用蒸镀方式制备无胶水层且厚度≤15μm的工艺设计和方法,实现了高性能高频换能器的生产国产化,提高了图像分辨率的同时优化了图像质量。
该配套产品使用高频率、宽带宽、高灵敏度的超声波成像,能够实现冠脉血管的扫描成像和血管直径测量,帮助医生判断病变严重程度及性质,有助于提高对冠状动脉病变的认识和指导介入治疗。
该配套产品的上市有利于降低临床治疗费用和该技术的临床应用推广,为PCI精准诊疗提供更好的诊断依据,制定更佳的治疗策略使患者受益。
(四十六)血管造影X射线机:该产品由高压发生器、X射线管组件、限束器、滤线栅、平板探测器、机架、导管床、显示器、显示器吊架、视觉组件、触控平板、控制模块、控制盒、脚踏开关、手闸、图像采集工作站、视频管理工作站、图像高级处理工作站、3D图像处理工作站和附件组成。适用于对血管造影检查、介入手术时提供X射线透视、摄影、血管减影图像和体层图像。
该产品采用9轴机器人DSA,能实现全腹部、全胸部的锥形束成像,解决了传统锥形束CT重建视野小的问题。此外,产品采用计算机视觉技术,实现了一键自动锥形束CT扫描和一键到位,可简化定位和锥形束CT的工作流,减少辐射暴露和术中操作步骤。与传统的医用血管造影X射线机相比,该产品可显著扩大锥形束CT重建视野,减少锥形束CT扫描的操作步骤、操作时间和辐射剂量,预期缩短成像前的准备时间,提高手术效率。
五、其他注册管理情况
(一)境内第二类医疗器械注册审批情况
2022年,各省级药品监管部门共批准境内第二类医疗器械注册32889项,与2021年相比增加4.4%。其中,首次注册13334项,与2021年相比增加2.2%。首次注册项目占全部境内第二类医疗器械注册数量的40.5%。
图17 境内第二类医疗器械注册形式比例图
延续注册10641项,与2021年相比减少6.9%,占全部境内第二类医疗器械注册数量的32.4%;变更注册8914项,与2021年相比增加26.6%,占全部境内第二类医疗器械注册数量的27.1%。
境内第二类医疗器械分项注册情况见图17。
从注册情况看,广东、江苏、北京、湖南、浙江、河南、山东、上海、湖北、安徽10省(直辖市)注册的境内第二类医疗器械数量较多。
第二类医疗器械注册具体数据见表1及图18。
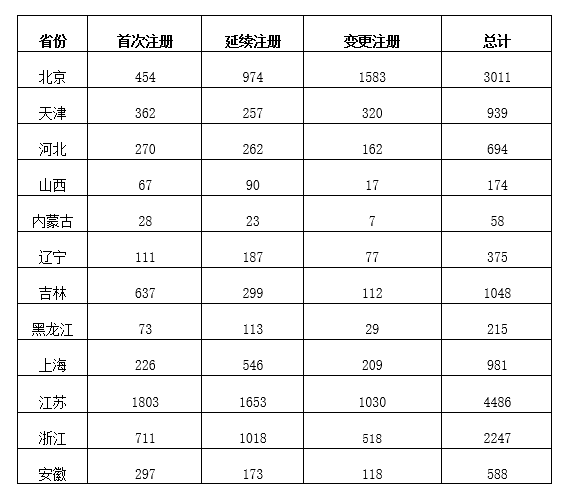

表1 境内第二类医疗器械注册表
从首次注册情况看,湖南、广东、江苏、浙江、山东、河南、吉林、浙江、湖北、广西10省(直辖市)首次注册的境内第二类医疗器械数量较多。各省第二类医疗器械首次注册数量排序图见图19。

图18 各省第二类医疗器械注册数据图

图19 各省第二类医疗器械首次注册排位图
(二)第一类医疗器械备案情况
2022年,国家药监局依职责共办理进口第一类医疗器械备案数量2023项,与2021年相比增加9.1%。
全国设区的市级药品监管部门依职责共办理境内第一类医疗器械备案数量28508项,与2021年相比增加6.5%。此外,2022年各省取消一类备案13917项。
(三)登记事项变更/变更备案情况
2022年,国家药监局依职责共办理进口第二、三类和境内第三类医疗器械变更备案5390项,与2021年相比增加17.1%。
其中,境内第三类医疗器械变更备案3435项,进口第二类、三类医疗器械变更备案1995项。
各省级药品监管部门依职责共办理境内第二类医疗器械变更备案11638项,与2021年相比增加8.5%。
(四)医疗器械临床试验机构备案情况
自2018年1月1日《医疗器械临床试验机构条件和备案管理办法》颁布实施以来,全国共计1177个机构完成了医疗器械临床试验机构备案工作,比2021年增加9.6%。
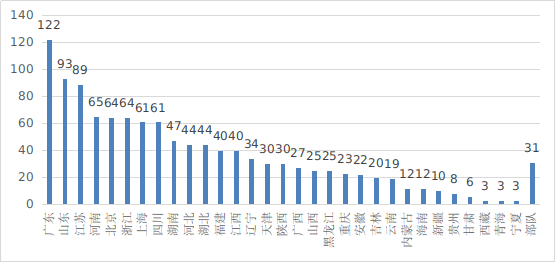
图20 全国医疗器械临床试验机构备案数量
其中广东、山东、江苏、河南、北京和浙江临床试验机构备案数量居全国前五名。全国医疗器械临床试验机构分布情况见图20。
注:本报告的数据统计自2022年1月1日至2022年12月31日。

