跳至内容
文章来源:器械市场雨
“高端医疗器械国产化率仍然较低,产业链发展不平衡不充分,关键技术、核心零部件进口依赖度较高。”
在今年的全国两会上全国人大代表、国药集团国药控股股份有限公司党委书记、董事长于清明提交了《关于大力支持高端医疗器械制造业发展的建议》等建议。
于清明建议,要大力支持高端医疗器械及其关键技术、核心零部件攻关进程,通过跨领域联合创新,加强国产器械质量品牌建设,鼓励临床推广应用,进一步推动医疗器械行业高质量发展。促进医疗器械国产替代,以高端医疗器械科技创新助力中国式现代化建设,满足人们对健康生活的新期待。
“我国医疗器械行业规模超万亿,但医疗器械产业链完整性、稳定性和竞争力不强。”
于清明介绍,一方面高性能医疗器械的国产化率仍然不高;另一方面,国内企业创新要素储备有限,从事关键零部件、重要原材料自主研发的企业较少。比如在ECMO(体外膜肺氧合机)用中空纤维膜、血液净化设备用透析膜、CT球管用真空高温轴承、防护产品用髙效过滤材料、植入性器械用可吸收降解材料等原材料产业存在短板和空白。
于清明建议,一是组织跨领域联合攻关,以科技创新夯实高端器械工业基础。高端医疗器械属于高新技术集成领域,创新要素、技术体系十分复杂。要推进航空航天、电子信息、核工业、船舶、通用机械、新材料等行业与医疗器械行业跨领域合作、跨行业融合创新。依托大型央企建立高端医疗器械创新联合体和制造基地,推动国家级技术研究中心、重点实验室,产业链上游原材料及关键零部件供应商、龙头生产企业和流通企业、第三方技术检测机构和知名医疗机构等建立联合创新平台,加强整机、原材料、零部件全产业链跨领域协同攻关。聚集创新发展要素、产业链优质资源,建立高端医疗器械制造基地,打造各细分领域的特色产业聚集带。
二是增加高端医疗器械制造业财政资金投入,设立高端医疗器械产业专项基金。大力支持发展前景较好的创新型企业,加大对关键技术、重要原材料、核心零部件创新研发企业的财政支持,集中力量破解制约产业链高质量发展的瓶颈。
三是提高产业集中度,强化质量品牌建设。我国医疗器械企业的头部效应还未形成。要积极引导企业提升质量体系、加强品牌建设、完善售后服务,提高国产高端医疗器械的市场竞争力和品牌影响力。支持具有技术储备和资金优势的企业强强联合、做大做强,引领行业高质量发展。
四是大力支持国产高端医疗器械推广应用。优先考虑将国产创新医疗器械纳入医保支付范围,在DRG/DIP应用和大型医疗设备配置许可证办理方面给予适当倾斜,鼓励国产替代和临床使用。加强政产学研医各领域紧密合作,持续开展迭代创新,保证产业链平衡发展,满足市场需求。
国产高端医疗器械发展备受社会各界关注,据上游新闻报道,今年全国两会,全国政协委员、重庆医科大学附属第一医院骨科主任黄伟准备了一份关于“推进医学领域科技成果转化”的提案。
黄伟认为,国产医疗产业的发展远跟不上市场的快速增长,尤其在高端医疗器械,其份额仍被跨国公司占据,进口产品在我国医疗器械市场的垄断率高达到70%到80%,而医疗创新转化效率的低下,则是导致目前被外资企业“卡脖子”的主要原因。
对此,黄伟建议,可成立创新转化公司,优化校企资源整合。鼓励具备创新转化条件的高校或者医院集成资源成立研发转化团队,集中知识产权与创新转化力量成立公司,以公司方式运营,为产学研提供架构保障,拓展合作边界,促进资源整合。
国家医保局答人大代表建议—— 多项政策利好创新医疗器械
2023年3月4日,第十四届全国人大一次会议开幕前夕,国家医保局发布了《对十三届全国人大五次会议第3298号建议的答复》,其中针对代表提出的进一步完善医保DRGs支付体系——关于医疗新技术问题,国家医保局给出明确答复,并且进一步支持创新医疗器械豁免”DRG"!
《答复》中,国家医保局对地方医保部门在试点工作中探索建立CHS-DRG付费支持医疗新技术的有关机制点名支持:
如北京市对于符合一定条件的药品、医疗器械及诊疗项目,纳入CHS-DRG 付费除外支付管理。
2022年7月,北京市医保局下发了《关于印发CHS-DRG付费新药新技术除外支付管理办法的通知(试行)》,首次提出了一项DRG除外支付办法,明确创新药、创新医疗器械、创新医疗服务项目可以不按DRG方式支付,单独据实支付。
创新医疗器械豁免DRG,对于医疗器械企业而言无疑是重大利好。此次国家医保局点名支持北京市医保局将创新医疗器械豁免DRG,传递出支持这项政策在全国大范围推广的信号。
此外,2022年8月24日,国家医保局发布了的对“十三届全国人大五次会议第8013号建议”的答复中指出将完善相关政策,指导各地及时将符合条件的创新医用耗材按程序纳入医保支付范围。
该答复是国家首次明确创新医用耗材的医保支付途径,大多数创新医疗耗材因无法纳入医保而发展受阻,国家医保局的回复将有效打通这一难点,助力创新医疗耗材高质量发展。
另外,国家医保局还指出,在集中带量采购过程中,由医疗机构根据历史使用量,结合临床使用情况和医疗技术进步确定需求量,并根据临床使用特征、市场竞争格局和中选企业数量等因素合理确定带量比例,在集中带量采购之外留出一定市场,为创新产品开拓市场提供空间。
紧接着2022年9月3日,国家医保局对外发布《国家医疗保障局对十三届全国人大五次会议第4955号建议的答复》,明确创新医疗器械尚不实施带量采购,因其使用尚未成熟,使用量暂时难以评估。
在集采猛击耗材水分的同时,国家医保局明确创新医疗器械豁免集采、纳入医保支付,无疑为相关企业和市场注入一针强心剂,也为创新医疗器械的临床使用和进一步发展奠定良好的基础。
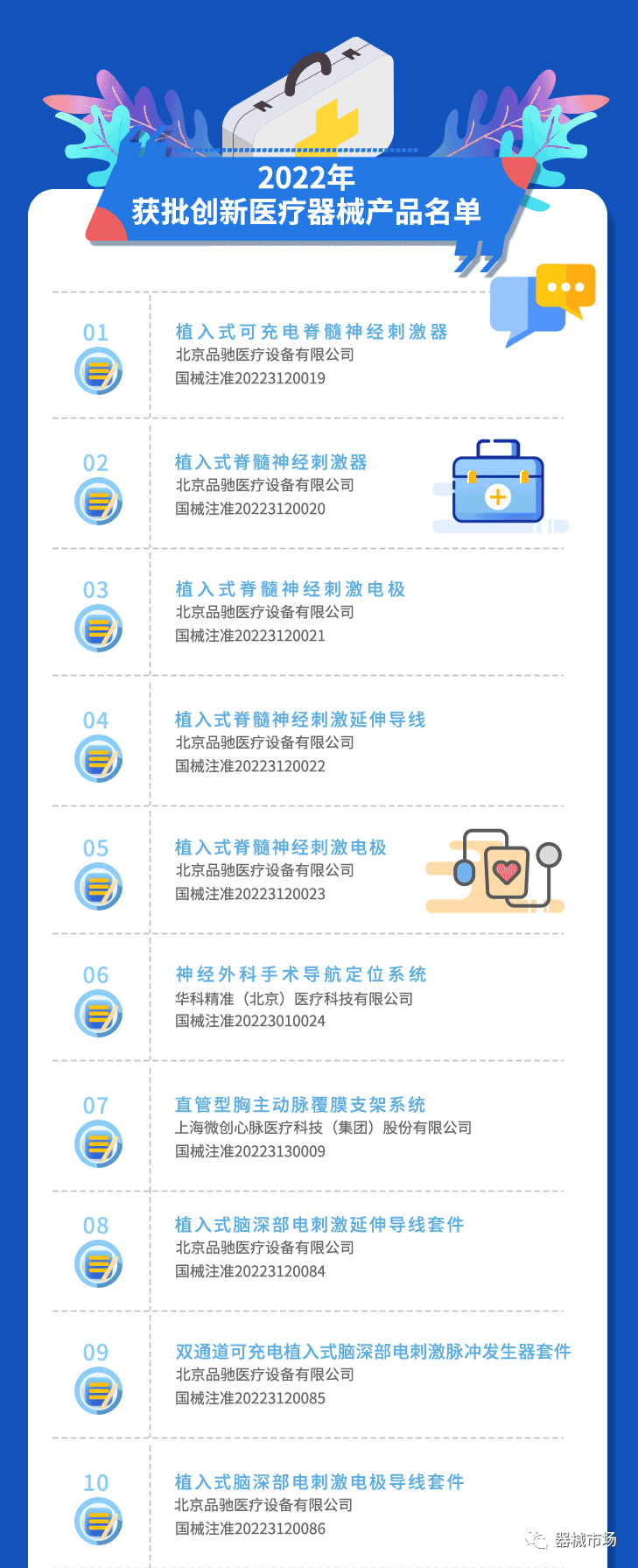
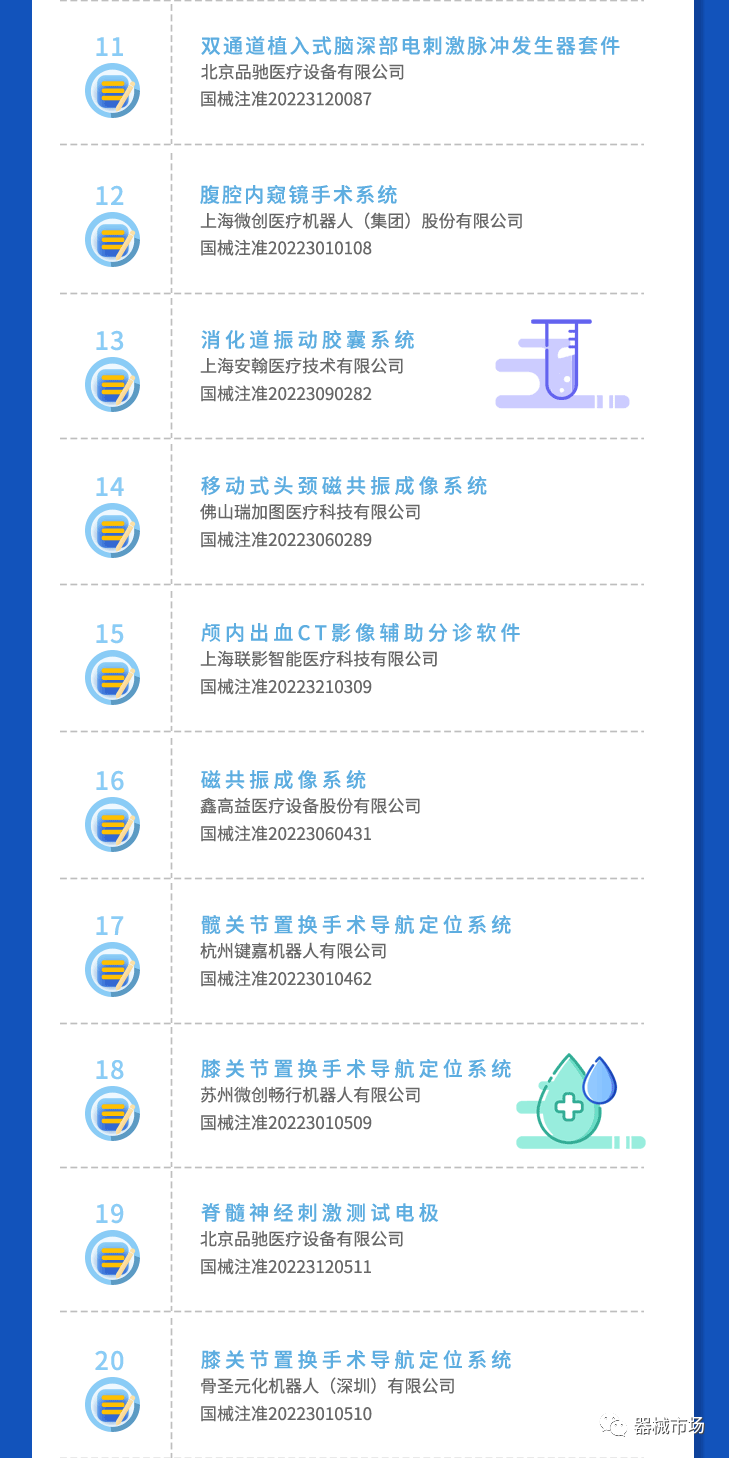
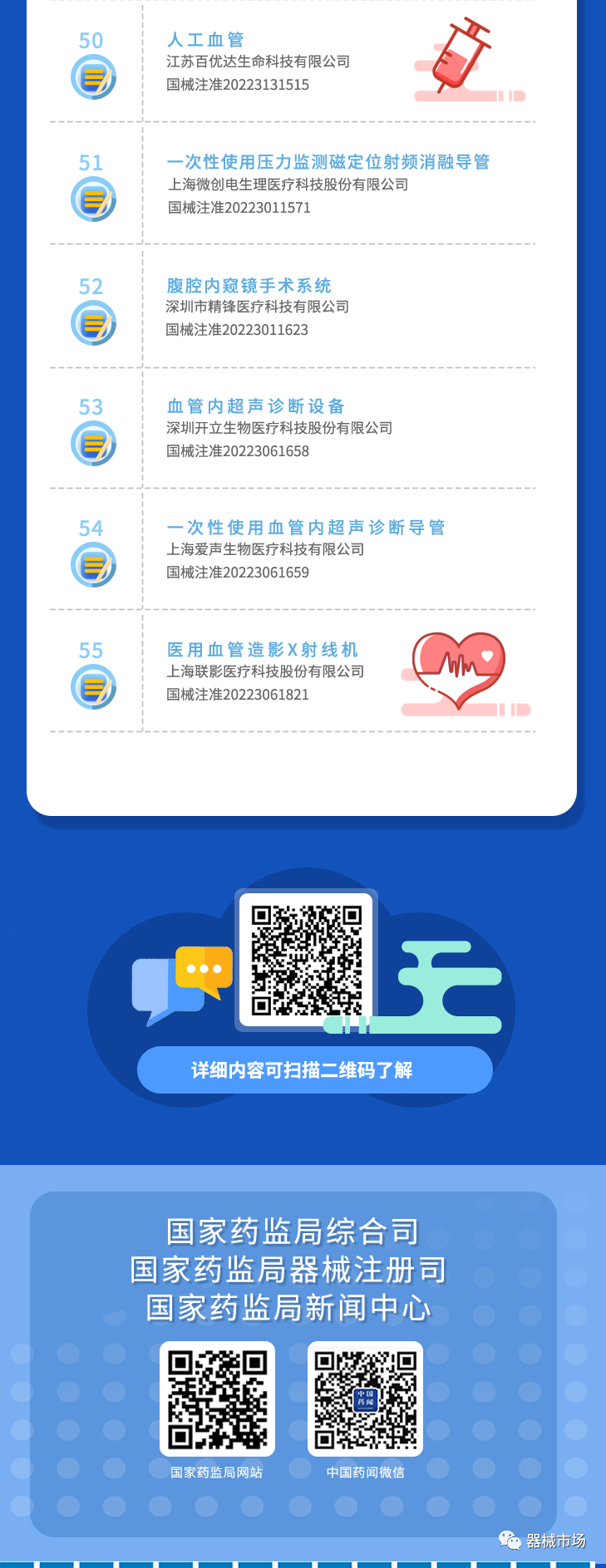
附:国家药品监督管理局发布:2022创新医疗器械注册审批创新高
医疗器械品类众多,可分为高值医用耗材、低值医用耗材、医疗设备、 IVD(体外诊断)四大类。根据使用场景和功能不同,高值医用耗材细分为骨科植入、血管介入、神经外科、眼科、电生理与起搏器等等。根据技术原理和功能差异,医疗设备可分为诊断设备(影像诊断如 DR、彩超、磁共振)、治疗设备 (各类手术器械、放射治疗机械)等;医疗器械细分领域虽差异巨大,但是每一个环节都需要其参与,医疗器械的制备涵盖高分子材料、电子、模具注塑、机械、生命科学等。欢迎加入艾邦医疗器械产业交流群探讨: